Atopijski dermatitis (AD)
Bolezen je pogosta, študije ocenjujejo da naj bi približno 10-20% vseh otrok imelo atopijski dermatitis, od teh pa se večini izrazi pred 2 letom starosti. Do pubertete pa večini (a ne vsem) bolezen izzveni. Približno 1-3% odraslih ima atopijski dermatitis. V 45% se prvi znaki pojavijo že v prvih 6 mesecih, v 60% v prvem letu, v 85% pa pred dopolnjenim 5 letom starosti.
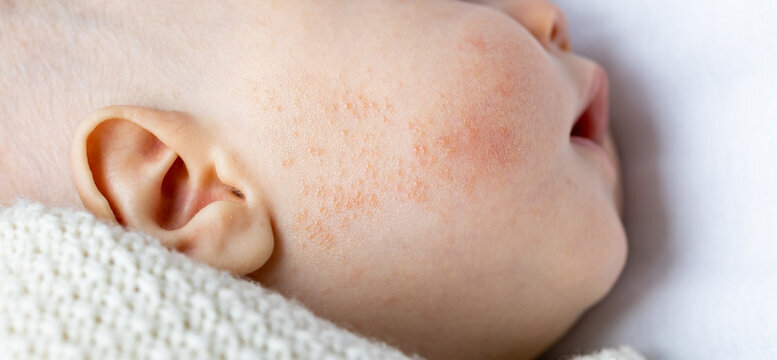
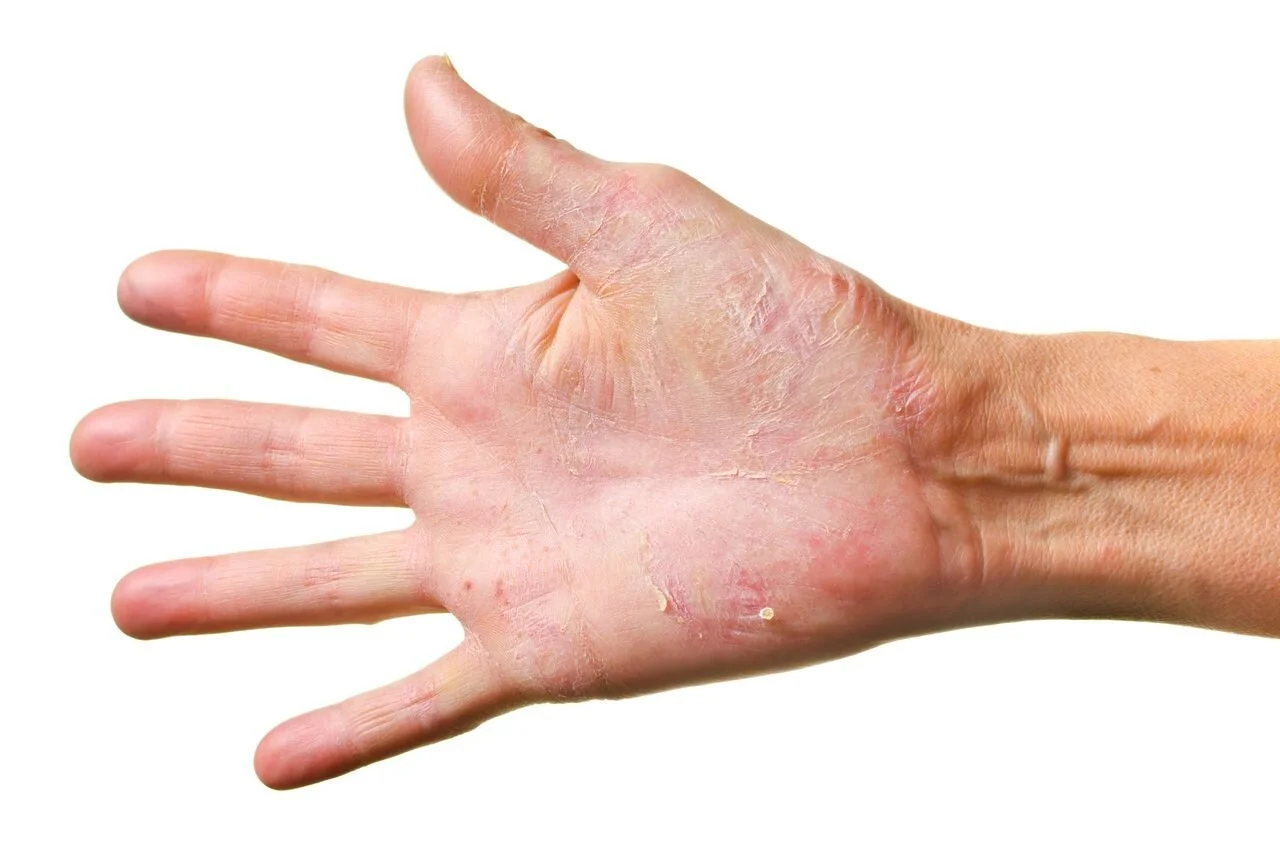
Pri dojenčkih je pogosto bolezen izražena na obrazu (licih), v otroštvu na upogibih okončin, v odrasli dobi pa na dlaneh.
Najbolj značilen znak klinične slike je rdečina in srbenje. Zelo intenzivna srbečica lahko vodi v poškodbe kože in moten spanec, Koža je izsušena, lahko je vidna motena desvkamacija (vidne so “luske”). V hujših primerih lahko postane “mokra”, prisotne so papule in kraste.
PATOGENEZA:
Patologija AD sestoji iz 3 glavnih komponent: Filagrina, serin proteaze in imunskega sistema.
Interakcija genetsko drugačnega imunskega sistema in nepravilnosti v stratum corneumu (zgornja plast povrhnjice) povzročijo pod pravimi okoljskimi pogoji hipersenzitivne reakcije na normalne zunanje dejavnike (elemente, snovi), njihov epidermis pa se ni sposoben braniti pred zunanjimi dejavniki tako kot pri ljudeh z zdravo kožo.
Na samo okvarjeno bariero stratum corneuma pa pri AD vplivajo: nepravilnosti filagrina, povečana aktivnost serine protease, zmanjšana količina ceramidov in ostalih lipidov stratum corneuma.
V nadaljevanju bom obravnala tri zgoraj omenjene dejavnike, značilne za atopijski dermatitis. Kljub temu, da jih bom obravnavala ločeno, se med seboj povezujejo in je ravno njihova interakcija ključna za potek AD. Skupaj vplivajo na spremenjen in nepravilen odziv kože na različne zunanje dejavnike; alergene, iritante, mikroorganizme in klimatske spremembe.
Vloga filagrina in bariera stratum corneuma
Vloga stratum corneuma (SC) je zaščita pred neželjenimi elementi iz okolja in ohranjanje vodnega ravnovesja. Ko ta kožna bariera pravilno deluje, je sposobna “dobre” elemente zadržati in preprečiti vstop “slabemu” ter prepoznati kaj je dobro, kaj potrebuje in kaj je “slabo”. To pomeni, da zdrav SC dovoli perkutano absorpcijo vode in ostalih hranil v kožo, prepreči odhod pomembnim sestavinam ki so v koži in prepreči škodljivim substancam in patogenim mikroorganizmov dostop do nižje ležečih plasti kože.
Za AD pa je značilna nepravilnost v SC, katero povzročijo napake v: filagrinu, serin proteazi, lipidih SC:
1.Filagrin:
Filagrin ima vpliv na hidratacijo kože, strukturno obrambo in pH.
Filagrin nastane iz profilagrina (fosfolirirana beljakovina). Poleg profilagrina se v citoplazmi stratum granolusoma (plast povrhnjice) nahajajo tudi lamelarna telesca (ogljikovi hidrati, lipidi, hidrolitični encimi), njigova vsebina se izloči v medceličnino SC.
V končni diferenciaciji (iz keratinocitov v korneocite) je profilagrin defosfoliziran in proteolitično razgrajen v filagrin. Ta proces regulira koncetracija kalcijevih ionov, serin proteaza in inhibitor te proteaze.
V spodnjih slojih SC se filagrin veže na citoskelet keratina in novo nastalo poroženelo ovojnico korneocita. Ta povezava med citoskeletom keratina, filagrinom in poroženelo ovojnico splošči korneocite. Ti so med seboj tesno povezani preko keratin-filagrin povezav, poroženele ovojnice in dezmosomov. Brez filagrina je omenjena struktura oslabljena, kar povzroči lažji prehod snovi v kožo in povišan TEWL (izgubo vode).
V zgornjih slojih SC ima pa filagrin drugačno vlogo: razgradi se na proste aminokisline, UCA kislino, pirolidinsko karboksilno kislino (PCA). Omenjene snovi poznamo z eno besedo kot NMF-je, naravne vlažilne faktorje, ki nase vežejo vodo in jo zadržijo v SC. Posledično pomagajo pri ohranjanju pH-ja, pravilnemu odluščenju celic in zmanjšanju kolonizacije patogenih bakterij. Brez filagrina🡪manjšte stevilo NMF🡪slabša sposobnost zadrževanja vode🡪motena deskvamacija (“luščenje” celic).
Pravilen razvoj filagrina je za SC ključnega pomena, za to pa je potrebno pravilno delovanje proizvodnje, proteolize in inhibicije proteolize.
FLG je genski zapis filagrina, njegova mutacija pa zaradi zgoraj omenjenih razlogov povzroči nepravilno sestavo SC, zmanjšano število NMF-jev, suho kožo in povišan TEWL.
Manjša količina vode pa posledično še bolj onemogoči oziroma zmanjša delovanje encimov oz. proteolizo filagrina, kar stanje v SC še dodatno poslabša. (gre za “začaran krog”, saj to zopet vodi v manjšo količino vode v SC🡪manjša aktivnost encimov-🡪manjša koičina vode🡪manjša aktivnost encimov…..)
Mutacija FLG gena in posledično pomanjkanje filagrina pri osebah z AD povzroči tudi bolj alkalen pH površine kože. Glavni faktorji, ki vplivajo na kisel pH zdrave kože (4.0 do 6.0) so razgradni produkti urokanske kisline, proste maščobne kisline in NHE1. Ker je pa pri AD pomankljaj NMFjev (tudi UCA) pride do povišanega pH-ja na površini kože. Ravno rahlo kisel pH pa naj bi potencialno preprečil kolonizacijo mikroorganizmov na koži in posledično zmanjšal tveganje za infekcijo patogenij bakterij. Klinične raziskave so tudi našle povezavo med višino (alkalnostjo) pH površine kože in intenzivnostjo simptomov bolezni (pacienti z višjim pH-jem površine kože so imeli intenzivnejše izraženo bolezen).
Zdrava koža ima (najverjetneje zaradi prostih aminokislin) puferske sposobnosti, kar pomeni da je sposobna kljub aplikaciji kozmetičnih izdelkov z alkalnim pHjem, lasten pH površine kože vrniti v “normalne” vrednosti. Zaradi pomanjkana filagrina (in s tem prostih aminokislin) pa koža pri AD nima tako dobre puferske sposobnosti.
Višji pH površine kože vodi v povečano aktivnost serin proteaze, povečano dovzetnost za okužbe, zmanjšano sekrecijo lipidov.
Povečana dovzetnost za okužbe: pod normalnimi pogoji, mora bakterija za preživetje na koži najprej premostiti kislo okolje na površini kože ter se izogniti odkritju in obrambi imunskega sistema. Pri AD je pa poleg nepravilnega pHja prisotna tudi nepravilnost v imunskemu sistemu, kar omogoča patogenim bakterijam lažje pogoje za preživetje. Pri 90% odraslih z AD so na koži prisotni S.aureus ( pri zdravih zgolj 5%, saj zdrava koža prepreči Staphylococcus aurues da bi postala del normalne mikrobne flore na koži). V in-vitro raziskavi so ugotovili da UCA in PCA (razgradni produkti filagrina) inhibirajo proliferacjo S.aureus-ravno tega pa pri AD primanjkuje.
Mutacija FLG gena pa ni prisotna pri vseh pacientih z AD (priblizno 50%), prav tako ne mutacija gena direktno pomeni nastanek AD. Mutacija lahko povzroči tako Ichthyosis vulgaris (IV) kot atopijski dermatitis. Na miših so opravili raziskavo kaj privede ob pomanjkanju filagrina do nastanka ene ali druge bolezni. Miši so na začetku kazale vse simptome IV in ne AD, vendar ko so jih izpostavili alergenom se je situacija spremenila. Poleg nastanka AD so opazili še dodatno poslabšanje bariere SC in dvig TEWL-a. Prišli so do ugotovitve, da je stik z alergenom (posledično IgE alergijska sensibilizacija) poleg oslabljene kožne bariere ključen za prehod iz IV v AD.
Poleg pomanjkanja filagrina vodijo v oslabljeno bariero in potencialno povečano alergijsko preobčutljivost tudi drugi faktorji; zmanjšana količina ceramidov in ostalih lipidov, spremenjeno razmerje med lipidi in pretirana aktivnost serin proteaze. Ne glede na vzrok oslabljene bariere, vsi faktorji vodijo v zmanjšano strukturno in funkcionalno celovitost SC, kar vodi v povečano izpostavljenost potencialnim antigenom in posledično do alergijske preobčutljivosti značilne za AD.
2. Serin proteaza (SP) in SC
Serin proteaza (SP) je pomemben del dogajanja v koži, in sprememba v njihovem delovanju povzroči nepravilnosti v SC.
Pri AD je SP aktivnost povečana:
Zaradi alkalnega pH-ja: ker SP optimalno deluje v alkalnem okolju. Ko se pH kože zviša se posledično zviša tudi aktivnost SP
Genskih mutacij SP-ja: lahko pride do A) mutacije, ki povzroči nastajanje serin proteaz odpornih na inhibicijo (v koži mora biti sodelovanje med SP in inhibitorji SP-nadzor aktivnosti, ker pa je pri AD SP odporen na inhibicijo, njegove aktivnosti nič ne zaustavi)
mutacije, ki povzroči da inhibitorji niso učinkoviti pri inhibiciji SP
Po prvi ali drugi mutaciji je rezultat enak: pride do nenadzorovane, neinhibirane in povečane serin proteaze, encimske aktivnosti.
Povečana SP povzroči oslabljeno bariero SC: pospeši razgradnjo korneodesmosomov (-> povišan TEWL in povečana perkutana absorpcija), povzroči nepravilno izgradnjo medcelične lipidne membrane, poviša TH2 vnetje,
Povečana SP aktivnost onemogoči pravilno izgradnjo medcelične lipidne membrane (epidermalni lipidi), ker zniža celotno količino lipidov: zmanjšajo sekrecijo lamelarnih telesc v stratum granulosum (vir epidermalnih lipidov v SC).
Povečano TH2 (celice pomagalke) delovanje in izločanje IL-4 povzroči zmanjšano sintezo ceramidov, loricrina (protein ki sestavja poroženelo ovojnico v SC), filagrina in desmogleina-3(gradi dezmosome).
3. Lipidi:
Naloga epidermalnih lipidov je ohranjanje kohezije SC, pomagajo pri reguliranju pretoka vode ter delujejo kot bariera pred infekcijo.
Glikozilceramidi, sfingomielini in fosfolipidi so prekurzorji lipidov in se nahajajo v lamelarnih telescih v SG. Preko encimov se pretvorijo v ceramide in proste maščobne kisline in potujejo v SC, kjer so poleg holesterola del epidermalnih lipidov.
Pri AD je znižana količina ceramidov in ostalih lipidov, kar je prisotno tako na žariščih kot na preostali koži. Pri ljudeh z AD je struktura, delovanje in bariera SC oslabljena tudi takrat, ko ne kažejo kliničnih znakov.
Pri AD ima poleg vseh prej omenjenih faktorjih velik pomen tudi stres, saj poveča količino glukokortikoidov. Ti pa delujejo inhibicijsko na proizvodnjo epidermalnih lipidov kar prav tako vodi v okvarjeno bariero.
4.Imunski sistem
Zgoraj omenjene spremembe v SC niso dovolj za nastanek vseh znakov AD. Nepravilnosti imunskega sistema imajo prav tako ključno vlogo pri nastanku. Ugotovljene imunske anomalije vključujejo: povečano vnetje zaradi TH2, povečano alergijsko preobčutljivost, trajno celjenje vnetij in oslabljeno nespecifično imunost.
Že prej omenjena povečana aktivnost SP ima velik vpliv na kožni imunski sistem. Stimulira sproščanje IL-1 iz korneocitov, kar povzroči vnetne odzive kože. Pri AD to pomeni TH2 aktivnost in posledično povišano aktivnost IgE.
Pri zdravi kože je odziv na poškodovano bariero, povišan TEWL in manjšo količino vode tak, da stimulira sekrecijo in proizvodnjo lipidov in njihovih prekurzorjev. Ker pa pri AD poškodovano stanje epidermisa traja dalj časa, pride do vnetnih odzivov tudi v globljih plasteh kože.
Okvarjena bariera ne vodi le v večjo aktivnost TH2, ampak tudi povečano izpostavljenost antigenom, kar še dodatno poveča TH2 aktivnost in posledično IgE in alergijsko preobčutljivost.
TH2 povzroči izločanje IL-4 in IL-13 in zmanjša količino antimikrobnih peptidov (AMP). Manjša količina AMPjev pomeni manjšo obrambo pred patogenimi mikrobi oziroma povzroči lažjo kolonizacijo (predvsem stafilokokne). To pa še dodatno spodbudi dvig IgE in alergijske senzibilizacije, potencialni toksini ki jih batkerije izločajo pa še dodatno poslabša in podaljša trajanje izrazenih žarišč na koži.
IL-4 pa dodatno oslabša bariero ker: zniža produkcijo ceramidov, loricrina, desmogleina in filagrina.
IL-4 in IL-13 prav tako povzročita aktivacijo CCL18 (vrsta citokina oz. kemokina, ki povzroči aktivnost IgE).
Trajno celjenje “ran”:
V zdravi koži rana povzroči obnovitev tkiva:imunske celice infiltritrajo predel kože , da zaustavijo vdor mikrobov. Temu sledi proliferacija matičnih celic, ki diferencirajo in zamenjajo poškodovano tkivo. Pri AD je tako dogajanje stalno: vnetje, proliferacija, ki pa vodi do “spongiosis” (medcelični edem).
SMERNICE KOZMETIČNE NEGE:
Kemični in ostali pilingi so načeloma odsvetovani. V kolikor pa je koža v dobrem stanju, se lahko počasi in postopoma poskusi tudi s pilingi.
V primeru, da je prisotno vnetje svetujem obisk zdravnika, da se stanje čimprej umiri.
Viri:
1) J. Levin, S. Friedlander, J. Q. Del Rosso, “Atopic Dermatitis and the Stratum Corneum Part 1: The Role of Filaggrin in the Stratum Corneum Barrier and Atopic Skin”. J Clin Aesthet Dermatol. 2013;6(10):16–22
2) J. Levin, S. Friedlander, J. Q. Del Rosso, “Atopic Dermatitis and the Stratum Corneum Part 2: Other Structural and Functional Characteristics of the Stratum Corneum Barrier in Atopic Skin”. J Clin Aesthet Dermatol. 2013;6(11):49–54
3) J. Levin, S. Friedlander, J. Q. Del Rosso, “Atopic Dermatitis and the Stratum Corneum Part 3: The Immune System in Atopic Dermatitis”. J Clin Aesthet Dermatol. 2013;6(12):37–44
4) S. Kapur, W. Watson, S. Carr, “Atopic dermatitis”. Allergy Asthma Clin Immunol. 2018; 14(Suppl 2): 52.